 Gjenbruk av cellens molekylære maskin-komponenter
Gjenbruk av cellens molekylære maskin-komponenter
Evolution News & Views 21 februar 2017
Bilde 1: Celle med anstands-proteiner, ved Huber og Hoelz via Caltech.
Som en plausibel forklaring på livets kompleksitet, dukket darwinistisk tankegang opp når cellebiologi var et stort rør. Samtidig som det vi vet om celler og celle-innhold dramatisk har bedret seg i detaljeringsgrad og fokus, blekner ortodoks evolusjonær tenkning tilsvarende i sin overtalelsesevne. Det er en lærdom av det vi skrev i går om molekylære maskiner -her, men de siste nyhetene på det temaet kan ikke bli omfattet av en enkelt artikkel, eller to. Derfor går vi videre til automatiserte sikkerhetsagenter, linjemontører, resirkulering, termostater, montører, inspektører, livvakter, og mer.
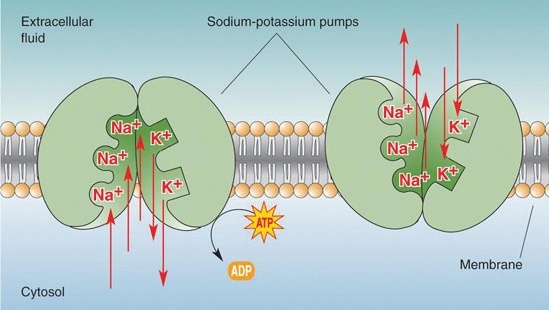 Tillegg om ionekanaler. Her er en annen ny artikkel om spenningsstyrte natriumkanaler, kalt Navs. Hos mennesker, er disse involvert i sensoriske nevroner samt hjerte- og hjerneceller, men selv mikrober har dem. Vi vil dele et rask sitat fra artikkelen i Nature Communications: "Traversering av Navs gjennom åpne, lukkede og inaktiverte tilstander, og deres tett koreograferte relasjoner med aktiviteter til andre ionekanaler, føret til utsøkt kontroll av intracellulære ione-konsentrasjoner i både prokaryoter og eukaryoter".
Tillegg om ionekanaler. Her er en annen ny artikkel om spenningsstyrte natriumkanaler, kalt Navs. Hos mennesker, er disse involvert i sensoriske nevroner samt hjerte- og hjerneceller, men selv mikrober har dem. Vi vil dele et rask sitat fra artikkelen i Nature Communications: "Traversering av Navs gjennom åpne, lukkede og inaktiverte tilstander, og deres tett koreograferte relasjoner med aktiviteter til andre ionekanaler, føret til utsøkt kontroll av intracellulære ione-konsentrasjoner i både prokaryoter og eukaryoter".
Dyktige linjemontører. Forskere ved Teknisk Universitet i Darmstadt -her, ble overrasket over å høre at maskinene som reparerer doble brudd i DNA-heliksen er "langt mer komplisert enn tidligere antatt." For eksempel, "Endene av brudd i dobbeltspiralen blir ikke bare sluttet, de endres først i en omhyggelig koreografert prosess slik at den opprinnelige genetiske informasjonen kan gjenopprettes. " Interessant at begge disse oppføringene refererer til koreografi - et flott design-ord .. - og forsterker virkningen med adjektivene utsøkt og omhyggelig.
'Ikke-noe-tull' anstand. Du kan se en annen maskin struktur i 3-D ved Caltech News , der artikkelen erklærer, "Protein anstand tar jobben sin på alvor." Hva er det? Det er et ribosomalt proteins hemmelige livvakt-tjeneste , i hovedsak:
"For proteiner, ville dette være det samme som den røde-løper behandlingen: hvert protein som tilhører den komplekse maskineriet i ribosomer - komponenter i cellen som produserer proteiner - har sin egen anstand for å lede det til rett sted til rett tid og beskytte den mot skade".
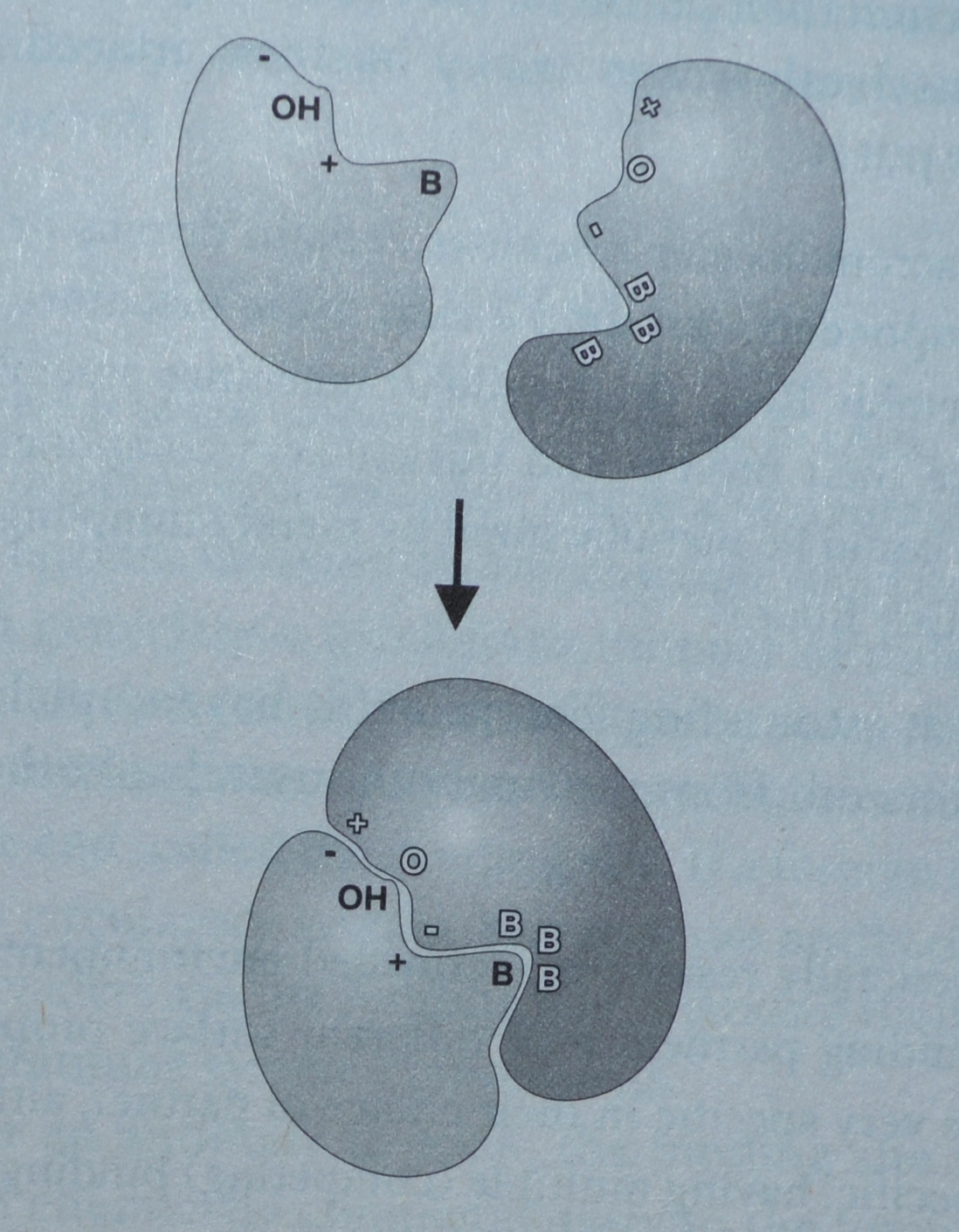
 Det spesielle proteinet de studerte, kalt L4, har en anstand som passer som 'hånd og hanske'. Når proteinet blir produsert i kjernen, tar anstanden det med på en lang reise ut kjerne-kanalen og inn i cytoplasma, hvor det må monteres inn i ribosomet på rett sted og tid. Underveis beskytter anstanden sin klient fra å bli hakket opp av "protein-oppstrimlings maskiner." Denne artikkelen er lastet med utrolige fakta. For eksempel:
Det spesielle proteinet de studerte, kalt L4, har en anstand som passer som 'hånd og hanske'. Når proteinet blir produsert i kjernen, tar anstanden det med på en lang reise ut kjerne-kanalen og inn i cytoplasma, hvor det må monteres inn i ribosomet på rett sted og tid. Underveis beskytter anstanden sin klient fra å bli hakket opp av "protein-oppstrimlings maskiner." Denne artikkelen er lastet med utrolige fakta. For eksempel:
"Å bygge ribosomer er en formidabel oppgave for cellen, som involverer ca 80 proteiner som utgjør ribosomet selv, strenger av ribosomalt RNA, og mer enn 200 proteiner i tillegg, som styrer og regulerer prosessen. "Ribosom montering er en dynamisk prosess, der alt skjer i en bestemt rekkefølge. Det er først nå vi begynner å belyse de mange skritt som er involvert," sier André Hoelz.
Det er et bilde av koreografi igjen. Et lite faktum hvis du ikke er imponert ennå: "Mer enn en million ribosomer produseres per dag i en dyrecelle." Dette er en stor ballett!
Bilde 3. Eks. på protein-passform
'Råkostkvernen'. Artikkelen ovenfor nevnte "protein-oppkuttings maskineri", så la oss se hva som er nytt om det. En europeisk team publiserte i Proceedings of the National Academy of Sciences at vi har lært at 26S Proteosomer, "en stor multisubunit kompleks som utfører degradering av intracellulære proteiner, merket for ødeleggelse," inneholder en "motor" med bevegelige deler. Denne motoren "bretter ut og flytter substrater inn i 20S kjerne-partikkelen" hvor proteinet blir oppsplittet, og tillater at dens aminosyrer kan resirkuleres. Hvordan vet maskinen hva som skal resirkulere? Feil kan bli katastrofale, ved å skade arbeidende proteiner. For riktig identifikasjon, tagger andre maskiner avfall med ubiquitin-molekyler. Proteosomet sjekker taggingen før det slipper proteinet til gjenvinnings-kassa. Vi har alle sett lastebilene som løfter søppelkasser opp i store containere og rister dem. Noe lignende foregår i cellen:
"Her rapporterer vi cryo-EM strukturer av gjær 26S proteosomet , i nærvær av forskjellige nukleotider og nukleotid-analogier, avslører eksistensen av fire forskjellige formgivnings/tilpasnings- tilstander. Disse strukturene belyser formgivnings/tilpasnings-endringer underliggende substrat forflytning og deres kobling med port-åpningen".
Dette er ingen gammeldags søppel-lastebil. Behandling innebærer flere trinn, åpninger, vendinger i en bestemt rekkefølge, som alle krever ATP for energi. "Vi antar at syklusen fortsetter inntil substrat-forflytnings prosessen er ferdig," sier de i konklusjonen. “Våre strukturer favoriserer en modell hvor hydrolysesyklusen forekommer i en sekvensiell orden rundt ringen i stedet for på en stokastisk måte." Interessant nok, én av de posisjoner kaller de "låseskive-konformasjon." Det kan godt være flere dansetrinn fra denne mobile roboten som ikke er oppdaget ennå..
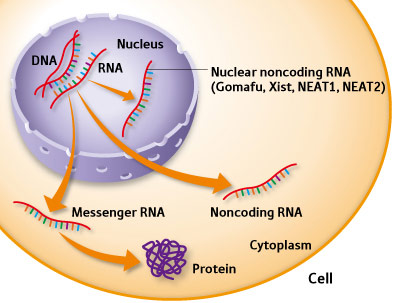 Inspektør-utkaster til unnsetning. I ribosomet, blir messenger RNA's oversatt til proteiner. Hva om mRNA har en skrivefeil? Hva om det mangler et stoppkodon? Det resulterende proteinet kan bli skadet, eller til og med være farlig. "Evnen til å kvitte seg med proteiner som enten er avvikende eller (i verste fall) giftige, er grunnleggende for en celles overlevelse, sier nyheter fra Charité Universitet iMedicine i Berlin . Forskere beskriver" rednings-proteiner "som patruljerer ribosomer, og gir den nødvendige kvalitets kontroll på samlebåndet. Det neste spørsmålet er: -hvordan gjenkjenner de feil?
Inspektør-utkaster til unnsetning. I ribosomet, blir messenger RNA's oversatt til proteiner. Hva om mRNA har en skrivefeil? Hva om det mangler et stoppkodon? Det resulterende proteinet kan bli skadet, eller til og med være farlig. "Evnen til å kvitte seg med proteiner som enten er avvikende eller (i verste fall) giftige, er grunnleggende for en celles overlevelse, sier nyheter fra Charité Universitet iMedicine i Berlin . Forskere beskriver" rednings-proteiner "som patruljerer ribosomer, og gir den nødvendige kvalitets kontroll på samlebåndet. Det neste spørsmålet er: -hvordan gjenkjenner de feil?
"Ved hjelp av Cryo-elektronmikroskopi for å studere strukturen til slike ribosom-mRNA komplekser, var forskerne i stand til å vise på hvilken måte spesielle rednings-proteiner (Dom34 og Hbs1) gjenkjenne slike fastlåste ribosomer, og dermed initiere en deling av anholdte komplekset og nedbrytning av det defekte mRNA. Rednings proteiner gjenkjenner anholdte ribosomer ved å oppdage, og binde seg til, konserverte steder normalt okkupert av mRNA. Denne direkte konkurranse-baserte tilnærming, sikrer at bare ribosomer med avvikende mRNA blir merket".
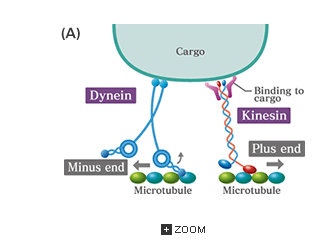 Stiftemaskinen. I korthet, en artikkel fra Ludwig Maximilian Universitetet i Munchen -her, beskriver protein-maskineri som festes til mRNA som de kommer ut av kjernen og stabiliserer dem for transport. "Vi ble overrasket over å se at RNA er ikke bare er gjenkjent av disse proteinene, de tvinger den også til å anta en ny form. De stifter dem sammen, så å si." Deretter tar motorproteiner "mRNA toget," bærer passasjeren ned cellens "jernbanelinjer," skriver artikkelen malerisk.
Stiftemaskinen. I korthet, en artikkel fra Ludwig Maximilian Universitetet i Munchen -her, beskriver protein-maskineri som festes til mRNA som de kommer ut av kjernen og stabiliserer dem for transport. "Vi ble overrasket over å se at RNA er ikke bare er gjenkjent av disse proteinene, de tvinger den også til å anta en ny form. De stifter dem sammen, så å si." Deretter tar motorproteiner "mRNA toget," bærer passasjeren ned cellens "jernbanelinjer," skriver artikkelen malerisk.
Bilde 5. DNA m-RNA og Protein
Bilde 6. Lasten festes til arbeiderne
Trykk-termostat. Hvordan opprettholdes riktig antall celler med epitelvev? -ønsket forskere ved 'University of Utah' å vite. Først fant de at enkle mekaniske spenninger påvirker balansen mellom fødsel og død. Når cellene blir for overfylt, fører interne press-krefter noen celler til å sprette ut av vevet og dø, gjennomgår apoptose-lenke. Når celler blir for få, trigger de hverandre til å utløse celledeling og dannelse av nye celler, for å fylle ut hullene. Men så oppdaget de et protein-maskin ansvarlig for denne balansen. Den kalles Piezo1, oppkalt utvilsomt for sin mekanist-sensitive natur, lik visse krystaller som kan gnistre når de er komprimert. De fant at Piezo1 "fungerer som en "termostat" på begge sider av cellen."Akkurat som en termostat regulerer både varme og kulde, er det fornuftig å ha én sensor som måler trengsel og strekk. Hvis det var to separate regulatorer, kan ting komme ut av kontroll ganske raskt, hvis en sensor ryker.
Fancy fotarbeid. Visste du at noen celler har føtter? Celler i immunsystemet, oppretter f. eks. om lag hundre "podosomer" (fot-kropper) for å bevege seg raskt til sine virke-områder. Podosomene skiller ut proteiner som bryter ned den ekstracellulære matrisen, slik at immunceller kan slippe gjennom fylt vev. Forskere ved 'National University of Singapore' -pdf; ønsket å lære mer om hvordan cellene danner disse små føttene. Det de fant var for komplisert å beskrive i detalj her, men det involverer flere proteiner som danner ringer, brytere og kontrollere, ved hjelp av de myosin-motorene vi lært om forrige gang.
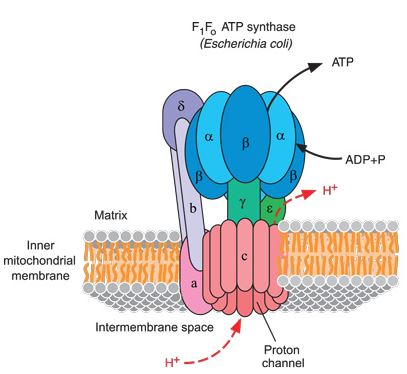
 Propellen. Vi mangler plass til å beskrive spiral-glidelåsen (Science Daily), DNA kirurgen og andre fascinerende maskiner, men vår mini-tour om det molekylære maskin-menasjeri ville ikke virke komplett uten noen nyheter om den ikoniske bakterieflagellen som var så innflytelsesrik i intelligent design bevegelsen. To nylige artikler kaster mer lys på flagellen, begge fra Osaka Universitet, en institusjon som har tatt ledelsen i å belyse denne propellens fysiske hemmeligheter i stor detalj. En nyhet fra Osaka Universitet -her, undersøker hvordan pH i systemet påvirker energien når cellen tvinger proteiner ut av proteinet, for å bygge maskinen. Små pH-microprober tillot teamet å "foreslå at eksport-apparatet bruker både ATP-hydrolyse samt H+ differensialer for å oppnå protein eksport."
Propellen. Vi mangler plass til å beskrive spiral-glidelåsen (Science Daily), DNA kirurgen og andre fascinerende maskiner, men vår mini-tour om det molekylære maskin-menasjeri ville ikke virke komplett uten noen nyheter om den ikoniske bakterieflagellen som var så innflytelsesrik i intelligent design bevegelsen. To nylige artikler kaster mer lys på flagellen, begge fra Osaka Universitet, en institusjon som har tatt ledelsen i å belyse denne propellens fysiske hemmeligheter i stor detalj. En nyhet fra Osaka Universitet -her, undersøker hvordan pH i systemet påvirker energien når cellen tvinger proteiner ut av proteinet, for å bygge maskinen. Små pH-microprober tillot teamet å "foreslå at eksport-apparatet bruker både ATP-hydrolyse samt H+ differensialer for å oppnå protein eksport."
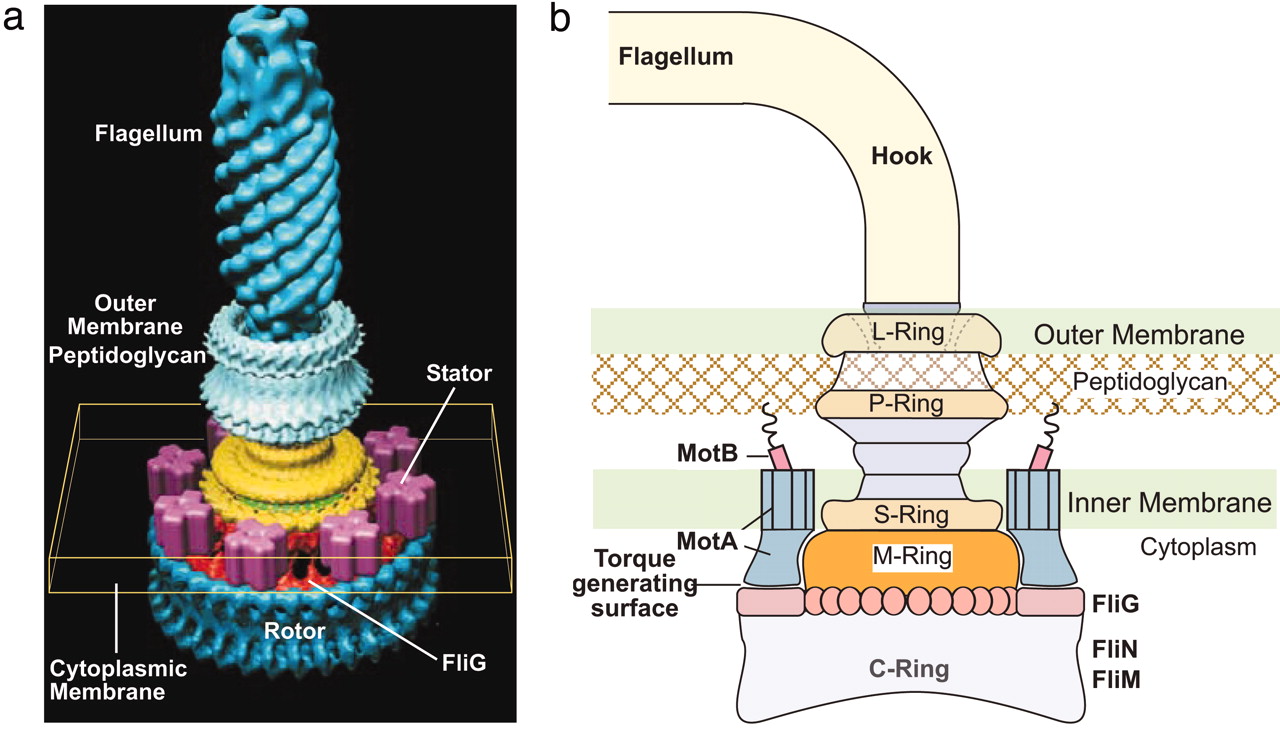
Den andre artikkelen, publisert av Nature Communications, utforsker nav og krokfeste-regioner av flagellen. Osaka forskere fant at "identiske folder" i subenhet-proteiner FlgE og FlgG blir brukt for distinkte mekaniske funksjoner" av nav og krokfeste-regioner, som er direkte forbundet med hverandre. Selv om disse to proteinene deler 39 prosent sekvensidentitet, har de forskjellige egenskaper: stangen er rett, mens kroken er fleksibel, slik at den bøyes som et universalledd. "Selv om disse to strukturene har samme spiralformede symmetri og gjentar avstand og nesten identiske folder av tilsvarende domener, avviker domene-orienteringen med -7°, noe som resulterer i tett og løs aksial subenhet-pakking i nav og krokfeste, henholdsvis, jfr. stivheten på navet og fleksibilitet til kroken, "forklarer de. "Dette er et godt eksempel på allsidig bruk av proteinstruktur i biologiske organismer." Det høres ut som godt design.
Bilde 7. Bakterie-flagell med nav og rotor
Som vi sa i forrige innlegg , er det ingenting som kan måle seg med å etterforske maskiner i detalj, for å forsterke den overbevisning at cellene er intelligent designet; de kunne ikke ha kommet av blinde prosesser av tilfeldige mutasjoner og naturlig utvalg. Noen av disse maskinene, når de muteres, fører til ødeleggende sykdommer, som ALS og kreft. Lite vet vi om hvor mye våre liv avhenger av nøyaktig, pålitelig virksomhet fra selve maskinene med bevegelige deler på nanoskala-nivå, som bærer uhyggelige likheter til maskinene vi kjenner på den menneskelige størrelses-skala: søppel-kompresser, varslings-systemer, propeller og mye mer.
For å 'låse opp livets mysterium' -lenke , sa Jed Macosko at det var "en rekke maskiner" i cellen, så mange som det finnes funksjoner i menneskekroppen. I 2017, 15 år senere, kan vi se at var ingen overdrivelse. De uklare glimt av maskiner som gjorde Michael Behe til en talsmann for intelligent design, har fortsatt makt til å inspirere en ny generasjon av unge forskere - enda så mye mer med økende oppløsning av avanserte bildeteknikker.
Oversatt av Asbjørn E. Lund
(Bildene sto ikke i opprinnelig artikkel, evt. untatt det 1., og er satt inn av undertegnede, se lenke i Bilde-nr)
 Gjenbruk av cellens molekylære maskin-komponenter
Gjenbruk av cellens molekylære maskin-komponenter Gjenbruk av cellens molekylære maskin-komponenter
Gjenbruk av cellens molekylære maskin-komponenter Tillegg om ionekanaler. Her er en annen ny artikkel om spenningsstyrte natriumkanaler, kalt Navs. Hos mennesker, er disse involvert i sensoriske nevroner samt hjerte- og hjerneceller, men selv mikrober har dem. Vi vil dele et rask sitat fra artikkelen i Nature Communications: "Traversering av Navs gjennom åpne, lukkede og inaktiverte tilstander, og deres tett koreograferte relasjoner med aktiviteter til andre ionekanaler, føret til utsøkt kontroll av intracellulære ione-konsentrasjoner i både prokaryoter og eukaryoter".
Tillegg om ionekanaler. Her er en annen ny artikkel om spenningsstyrte natriumkanaler, kalt Navs. Hos mennesker, er disse involvert i sensoriske nevroner samt hjerte- og hjerneceller, men selv mikrober har dem. Vi vil dele et rask sitat fra artikkelen i Nature Communications: "Traversering av Navs gjennom åpne, lukkede og inaktiverte tilstander, og deres tett koreograferte relasjoner med aktiviteter til andre ionekanaler, føret til utsøkt kontroll av intracellulære ione-konsentrasjoner i både prokaryoter og eukaryoter".
 Det spesielle proteinet de studerte, kalt L4, har en anstand som passer som 'hånd og hanske'. Når proteinet blir produsert i kjernen, tar anstanden det med på en lang reise ut kjerne-kanalen og inn i cytoplasma, hvor det må monteres inn i ribosomet på rett sted og tid. Underveis beskytter anstanden sin klient fra å bli hakket opp av "protein-oppstrimlings maskiner." Denne artikkelen er lastet med utrolige fakta. For eksempel:
Det spesielle proteinet de studerte, kalt L4, har en anstand som passer som 'hånd og hanske'. Når proteinet blir produsert i kjernen, tar anstanden det med på en lang reise ut kjerne-kanalen og inn i cytoplasma, hvor det må monteres inn i ribosomet på rett sted og tid. Underveis beskytter anstanden sin klient fra å bli hakket opp av "protein-oppstrimlings maskiner." Denne artikkelen er lastet med utrolige fakta. For eksempel: Inspektør-utkaster til unnsetning. I ribosomet, blir messenger RNA's oversatt til proteiner. Hva om mRNA har en skrivefeil? Hva om det mangler et stoppkodon? Det resulterende proteinet kan bli skadet, eller til og med være farlig. "Evnen til å kvitte seg med proteiner som enten er avvikende eller (i verste fall) giftige, er grunnleggende for en celles overlevelse, sier nyheter fra Charité Universitet iMedicine i Berlin . Forskere beskriver" rednings-proteiner "som patruljerer ribosomer, og gir den nødvendige kvalitets kontroll på samlebåndet. Det neste spørsmålet er: -hvordan gjenkjenner de feil?
Inspektør-utkaster til unnsetning. I ribosomet, blir messenger RNA's oversatt til proteiner. Hva om mRNA har en skrivefeil? Hva om det mangler et stoppkodon? Det resulterende proteinet kan bli skadet, eller til og med være farlig. "Evnen til å kvitte seg med proteiner som enten er avvikende eller (i verste fall) giftige, er grunnleggende for en celles overlevelse, sier nyheter fra Charité Universitet iMedicine i Berlin . Forskere beskriver" rednings-proteiner "som patruljerer ribosomer, og gir den nødvendige kvalitets kontroll på samlebåndet. Det neste spørsmålet er: -hvordan gjenkjenner de feil? Stiftemaskinen. I korthet, en artikkel fra Ludwig Maximilian Universitetet i Munchen -her, beskriver protein-maskineri som festes til mRNA som de kommer ut av kjernen og stabiliserer dem for transport. "Vi ble overrasket over å se at RNA er ikke bare er gjenkjent av disse proteinene, de tvinger den også til å anta en ny form. De stifter dem sammen, så å si." Deretter tar motorproteiner "mRNA toget," bærer passasjeren ned cellens "jernbanelinjer," skriver artikkelen malerisk.
Stiftemaskinen. I korthet, en artikkel fra Ludwig Maximilian Universitetet i Munchen -her, beskriver protein-maskineri som festes til mRNA som de kommer ut av kjernen og stabiliserer dem for transport. "Vi ble overrasket over å se at RNA er ikke bare er gjenkjent av disse proteinene, de tvinger den også til å anta en ny form. De stifter dem sammen, så å si." Deretter tar motorproteiner "mRNA toget," bærer passasjeren ned cellens "jernbanelinjer," skriver artikkelen malerisk. Propellen. Vi mangler plass til å beskrive spiral-glidelåsen (Science Daily), DNA kirurgen og andre fascinerende maskiner, men vår mini-tour om det molekylære maskin-menasjeri ville ikke virke komplett uten noen nyheter om den ikoniske bakterieflagellen som var så innflytelsesrik i intelligent design bevegelsen. To nylige artikler kaster mer lys på flagellen, begge fra Osaka Universitet, en institusjon som har tatt ledelsen i å belyse denne propellens fysiske hemmeligheter i stor detalj. En nyhet fra Osaka Universitet -her, undersøker hvordan pH i systemet påvirker energien når cellen tvinger proteiner ut av proteinet, for å bygge maskinen. Små pH-microprober tillot teamet å "foreslå at eksport-apparatet bruker både ATP-hydrolyse samt H+ differensialer for å oppnå protein eksport."
Propellen. Vi mangler plass til å beskrive spiral-glidelåsen (Science Daily), DNA kirurgen og andre fascinerende maskiner, men vår mini-tour om det molekylære maskin-menasjeri ville ikke virke komplett uten noen nyheter om den ikoniske bakterieflagellen som var så innflytelsesrik i intelligent design bevegelsen. To nylige artikler kaster mer lys på flagellen, begge fra Osaka Universitet, en institusjon som har tatt ledelsen i å belyse denne propellens fysiske hemmeligheter i stor detalj. En nyhet fra Osaka Universitet -her, undersøker hvordan pH i systemet påvirker energien når cellen tvinger proteiner ut av proteinet, for å bygge maskinen. Små pH-microprober tillot teamet å "foreslå at eksport-apparatet bruker både ATP-hydrolyse samt H+ differensialer for å oppnå protein eksport."