Nano-molekylære motorer
(fra kap. 10 i boka: By Design av Dr. Johathan Sarfati)
 Den levende verden inneholder overraskende nok skikkelige elektriske, rotasjonsmotorer. For evolusjonister som forutsa at hjul ikke kunne eksistere, fordi de ikke kunne ha utviklet seg gradvis, må de være et tankekors. Motorene i den levende verden, er perfekte eks. på den ultimate nano-teknologi. Biosfæren har også en variasjon av lineære motorer, som er like problematiske for evolusjonsteorien. I noe banebrytende forskning benyttes biologiske motorer for å assistere menneske-tilvirket nanoteknologi, som for tiden er primitiv sammenlignet med maskiner i biosfæren.
Den levende verden inneholder overraskende nok skikkelige elektriske, rotasjonsmotorer. For evolusjonister som forutsa at hjul ikke kunne eksistere, fordi de ikke kunne ha utviklet seg gradvis, må de være et tankekors. Motorene i den levende verden, er perfekte eks. på den ultimate nano-teknologi. Biosfæren har også en variasjon av lineære motorer, som er like problematiske for evolusjonsteorien. I noe banebrytende forskning benyttes biologiske motorer for å assistere menneske-tilvirket nanoteknologi, som for tiden er primitiv sammenlignet med maskiner i biosfæren.
Den evolusjonære gåten
J.B.S. Haldane erklærte i 1949 at evolusjon aldri kunne ha produsert 'varierende mekanismer, likt hjulet og magneten, som ville være unyttige inntil de var temmelig ferdigstilt'. (1) Derfor ville slike maskiner i organismer, etter hans mening, vise at evolusjonsteorien var feilaktig. Funnet av slike molekylære motorer har oppfylt ett av Haldanes kriterier. Som vist i kap. om navigering, den mengden av skapninger som benytter magnetiske sensorer for navigering, har oppfylt Haldanes 2. kriterium. Men mange evolusjonister siler á priori ut design, så bevisene, selv om de er overveldende, ville automatisk bli avvist.
Bilde 1. Forsøk på definisjon av molekylære maskiner
Motorer
Motorer er irreduserbart komplekse, fordi de trenger mange samvirkende deler til å fungere. En elektrisk motor trenger f.eks. en kraftkilde, en bevegelig rotor, en fast stator, osv. Desto flere deler som trengs for en maskin, desto hardere er det å gjøre den mindre. Mikro-miniatyrisering er en viktig del av computer industrien, og de beste menneskelige sinn arbeider konstant med det. Og selv om miniatyriserte motorer ville være svært nyttige for å åpne b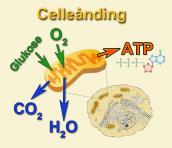 lokkerte arterier og blod-rensing, så gjør antall deler det vanskelig å lage dem, under en viss størrelse. Men oppfinnsomme ingeniører gjør dem mindre hele tiden (2).
lokkerte arterier og blod-rensing, så gjør antall deler det vanskelig å lage dem, under en viss størrelse. Men oppfinnsomme ingeniører gjør dem mindre hele tiden (2).
Bilde 2. Celleånding gir ATP
Verdens minste motor: ATP-syntase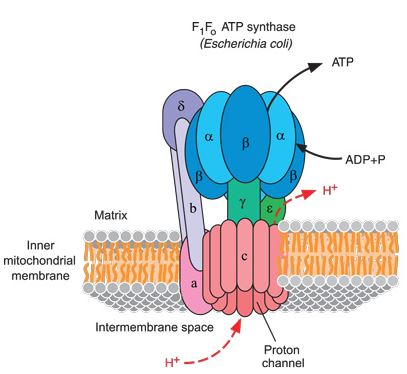
En artikkel publisert i Nature, mars 1997, annonserte oppdagelsen av den minste motor i universet (4). En kommentar i samme magasin, ble kalt 'virkelige skapte motorer' (5). Hiroyuki Noji et al. observerte da direkte rotasjonen til enzymet F1-ATPase, en underenhet av ett større enzym, ATP-syntase (6). F1 enheten beveger seg utenfor en membran, mens den andre delen er inni membranen, Fo (7).
Rotasjons energi hadde tidligere blitt foreslått som mekanisme for enzym-aktivitet av Paul Boyer, noe som innebar at enzymet fungerte som en motor (8). Strukturell bestemmelse av røntgen-stråle difraksjon, av ett team ledet av John Walker, hadde støttet denne teorien (9). Noen få måneder etter Noji et al. publiserte sitt arbeid, ble det annonsert at Boyer og Walker hadde vunnet halvparten av Nobelprisen i kjemi (1997), for sin oppdagelse (10). F1-ATPase motoren, har ni komponenter, fem ulike proteiner. F1-ATPase motoren er en utflatet halvkule ca. 10 nm diameter, 8 nm høy, så liten at det ville ta 10 opphøyd i 17 av dem, å fylle volumet til ett knappenålshode. Denne har vist seg å spinne lik en motor som for å produsere ATP, ett kjemikalie som er livets energi-enhet.
Etter størrelsen produserer denne motoren en umåtelig snu-kraft. I eksperimentet til Noji et al, roterte den langs et annet protein (actin), 100 ganger sin egen lengde, tilstrekkelig til å muliggjøre observasjon av rotasjonen, med et kraftig mikroskop. Når den frakter tung last, skifter den sannsynligvis til ett lavere gir. Uten denne lasten roterer den ca. 10.000 rotasjoner pr. minutt. Til forskjell fra mange menneskelagde motorer, som er laget av negativt ladde elektroner, så er ATP-syntase drevet fram av positivt ladde protoner (hydrogen ioner-H+). ATP-syntase inneholder også Fo enheten, som inneholdt i membranen, fungerer som en proton-kanal. Protonene som flyter gjennom kanalen, forårsaker at en hjul-lignende struktur går rundt, liksom vann driver et skovlhjul.
ATP-syntase er det sentrale enzymet i energi omdannelse i mitokondriene. De er innhyllet i folder i mitokondrienes innerste membraner, kloroplast og bakterier.
Hvordan rotasjon danner ATP
En rotasjon produserer tre nye ATP-molekyler. Etter tur, benyttes ti protoner for hver rotasjon, som innebærer at det må være eksakt ti 'c'-subenheter i rotoren til Fo-enheten (i bunnen av Bilde 3) -ellers vil den ikke virke (11). Dette forholdet 10:3 innebærer at det er nok et kompleksitets-nivå for evolusjon å forklare, noe som de har avholdt seg fra.
Syntesen avhenger av tre kjemiske identiske regioner, som hver har tre 3-dim. arrangement for katalyse-reaksjoner: Løs (L), tett (T) og Åpen (Å). L kan holde de to reaksjonspartnerne omvendt kompatible. I T konfigurasjon er reaksjonspartnerne bundet så tett at ATP er dannet. Men i Å-konfigurasjon, er bindingen svak nok til å frigjøre ATP som allerede er dannet i T-tilstanden. Så produksjon av ATP innebærer endring av tilpasningen ved hver gitt tilstand fra L til T til Å, og så starte ny syklus med L igjen. Dette oppnås ved rotasjon av den assymetriske sentral-'stengelen' (stalk), som roterer i etapper på 120 grader (1/3 dels omdreining) (13), og danner internt skifte av tilstandene (14). Ulikt de fleste enzymer, der energi trengs for å linke byggestenene, benytter ATP-syntesen energi for å linke dem til enzymer, og kaste bort nylig dannede ATP molekyler. Å separere ATP fra enzymer krever mye energi.
Kraften som driver protonene er et annet 'lag' med kompleksitet. Kjemisk energi i mat blir frigitt via oksidering i den såkalte Krebs-syklusen. Dette frigjør høy-energi elektroner, og deres energi fanges av spesialiserte molekyler i den elektroniske transport-kjeden. Denne energien produserer en elektrokjemisk gradient, som likner ett batteri. Men i dette tilfellet frigjøres energi ved å drive protoner på tvers av en membran. Dette er nødvendig for å skape proton-gradienten som driver ATP-syntesen. Hele systemet trenges. ATP står for Adenosintrifosfat. Det er en høyenergi sammensetning, og frigjør energi ved å tape en fosfat-gruppe, som ADP, Adenosin difosfat. Energi er essensiell for livet, og alt liv benytter ATP som sin energi-enhet (15). Selv bakterier og mikroorganismer har ATP-syntese motorer. Dette gjør sannsynligvis ATP til det mest allesteds-nærværende protein på jorda. Den menneskelige kropp generer omtrent sin egen vekt i ATP pr dag, dannet ved billioner av disse ATP-motorene. Og den forbrukes meget raskt til å gi kraft til vitale biokjemiske reaksjoner, inklusive DNA og protein-syntese, muskel-sammentrekning, næringstransport og nerveimpulser. En organisme uten ATP er som en bil uten energi. Cyanid er nettopp så giftig, fordi den stopper produksjon av ATP.
Evolusjon av ATP-syntese?
Denne motoren har mange komponenter som trenger å være fullt sammensatt, før de kan virke i det hele tatt. Spesielt den 10-foldige symmetrien til Fo-karusellen, har ingen funksjon i seg selv. Og den trefoldige symmetrien til F1-'sopphatten', med akkurat de riktige molekylære arrangement til å gi tre mulige tilpasninger, (L,T og Å), ville være unyttige uten den roterende 'akselen' som endrer tilpasningene. Og motoren ville heller ikke fungere, uten proton-kanalen på rett plass. Motoren fungerer bare fordi dens komponenter er korrekt organisert. OM en sammenligner med en elektrisk motor, så forklarer ikke eksistensen av elektrisk ledning, børster og magneter hvordan de ble organisert for å danne en motor. Noen evolusjonister har spekulert i at F1-sektoren kunne ha oppstått via en viss klasse enzymer (helicase) , som er vitale for alle organismer. Begrunnelsen er noe delt ensartet oppbygning (homologi) og at forskning har vist at 'helicase' er en aktiv (unwinding) 'utrullingsmotor' (16). DNA-kjeden skulle da formodentlig være analog til gamma-kjeden i ATP-syntasen. Imidlertid benytter helicase-operasjonen i seg selv ATP, så hvordan kunne denne formodede forgjengerne ha fungert i det hele tatt?
Siden energi er helt vital for livet, så kunne ikke livet ha blitt til før denne motoren var fullt funksjonell. Naturlig seleksjon er pr. definisjon en differential-reproduksjon, som krever selv-reproduserende enheter fra starten av. Men selv-reproduksjon krever ATP for å få energi. Om alle mellomsteg skulle mangle energi, ville de være døde.
Bakterie-flagellen: drevet av en elektro motor
Våre tarmer er fulle av bakterier, f.eks. E-coli bakterier. Denne mikroben er bare 2 mikrometer( 0,002 mm) lang, med en cellevegg på ca. 30 nm (nanometer-milliontedels-meter) og dens masse er bare 1 picogram, og inneholder ca. 70% vann(18). Ikke til å undres over at biologer i Darwins tid avskrev slike celler som ' dråper med cytoplasma'. Imidlertid er hver levende organisme en astronomisk komplisert, selv-reproduserende maskin (senere i kap. 11). Koden for instruksjonene til å bygge E-coli omfatter over 4,6 millioner basepar, som spesifiserer nesten 4.300 gener, hvorav de fleste koder for proteiner (14).
Utenbords motorer
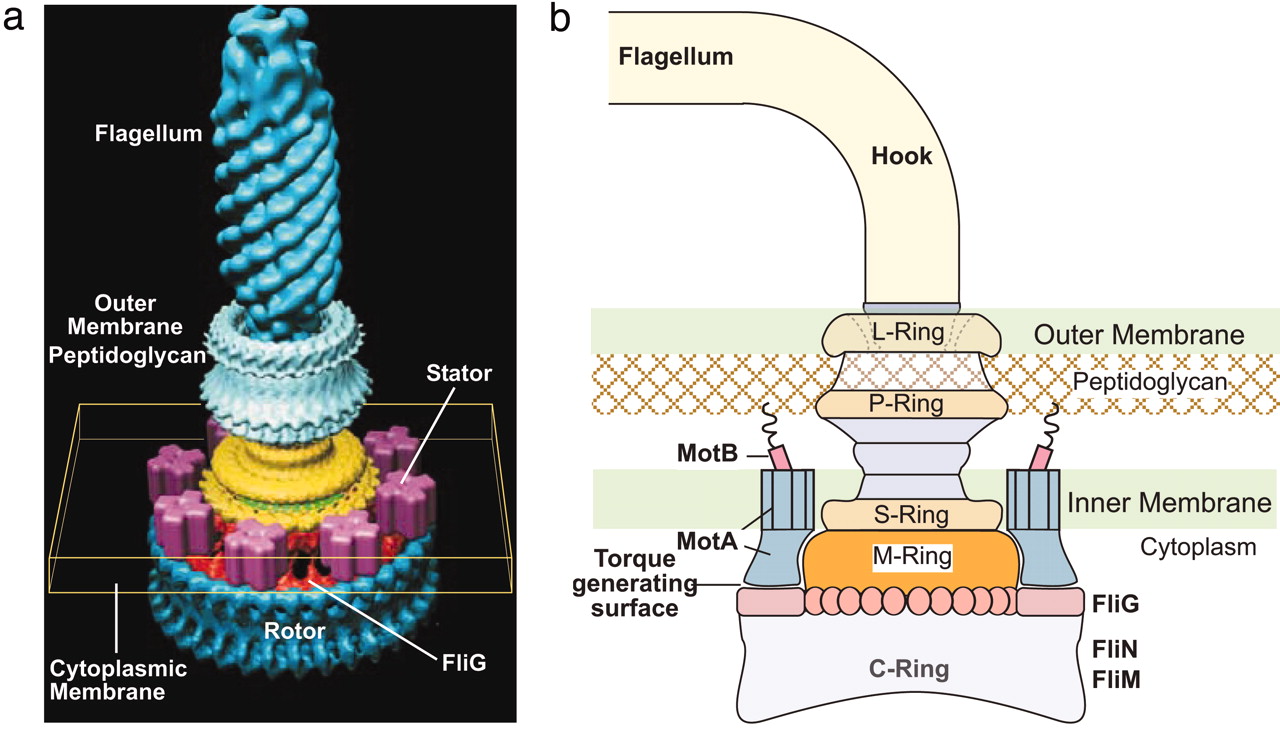 Bakterien drives ved hjelp av reelle elektriske, utenbords-motorer, som bare er 45 nanometer i diameter (14). Disse motorene er forbundet med lange, tynne, pisk-lignende skrueformede tråder, som er flere ganger lengre enn mikroben, via ett universal-ledd. Dette omgjør den roterende bevegelsen til en bølgeliknende bevegelse i tråden. Motoren innbefatter en stator, rotor, drivaksel og en hylse som leder drivakselen ut av celleveggen. Samlingen av motor og tråd kalles en bakterie-flagell (14). Cellen har flere flageller og deres samvirkende fremdrift tillater cellen å svømme 35 cellers lengde pr. sekund (14). I likhet med ATP-syntase motoren blir den drevet av en proton-flyt, denne gang fra utsiden til innsiden av delen (unntatt marine-bakterier og bakterier i meget alkaliske betingelser, der sodium-ioner benyttes i stedet.) Protonene drivers enten av en elektrisk eller en pH-gradient, og energien til å drive den er fra oksidasjon av næringen dens. Proton-flyten endrer formen til én av deres stator-proteiner, som utvirker en kraft på en av rotor-proteinene, og derved driver rotoren rundt (14).
Bakterien drives ved hjelp av reelle elektriske, utenbords-motorer, som bare er 45 nanometer i diameter (14). Disse motorene er forbundet med lange, tynne, pisk-lignende skrueformede tråder, som er flere ganger lengre enn mikroben, via ett universal-ledd. Dette omgjør den roterende bevegelsen til en bølgeliknende bevegelse i tråden. Motoren innbefatter en stator, rotor, drivaksel og en hylse som leder drivakselen ut av celleveggen. Samlingen av motor og tråd kalles en bakterie-flagell (14). Cellen har flere flageller og deres samvirkende fremdrift tillater cellen å svømme 35 cellers lengde pr. sekund (14). I likhet med ATP-syntase motoren blir den drevet av en proton-flyt, denne gang fra utsiden til innsiden av delen (unntatt marine-bakterier og bakterier i meget alkaliske betingelser, der sodium-ioner benyttes i stedet.) Protonene drivers enten av en elektrisk eller en pH-gradient, og energien til å drive den er fra oksidasjon av næringen dens. Proton-flyten endrer formen til én av deres stator-proteiner, som utvirker en kraft på en av rotor-proteinene, og derved driver rotoren rundt (14).
Bilde 4. Bakterieflagellen
Kunne den ha utviklet seg?
Scientific American forsøkte å forklare opphavet til den forbløffende miniatyr-motoren, ved å hevde at delene var samvirket fra andre funksjoner, spesielt type III av det utsondrende systemet (TTSS) til noen sykdoms-bakterier (19). TTSS er et helt annerledes apparat, brukt av visse bakterier til å sprøyte gift inn i andre bakterier. TTSS er sammensatt av proteiner som ligner på noen av dem i bakterieflagellen. Scientific Americans argument som kommer fra Kenneth Miller (20), og er blitt gjentatt av Richard Dawkins (21), er som å hevde at om komponentene til en elektrisk motor allerede eksisterer, så kan de samle seg selv til en fungerende motor. Imidlertid er rett organisering like viktig som de rette komponentene. Scott Minnich ved universitetet i Idaho, en ledende ekspert på flagellar-motoren, var uenig med Miller. Han sier hans oppfatning er at motoren er intelligent designet, og har gitt ham mye forsknings-innsikt. Minnich påpeker at selve sammensetnings-prosessen med 'i rett sekvens å sette sammen komponentene', krever andre regulerende maskiner (22). Han påpeker også at bare ca. 10 av de omkring 40 komponentene mulig kan forklares ved samhandling, men de 30 andre er helt nye. Videre viser Dr. Minnichs forskning at bakterie-flagellen ikke vil dannes ved over 37 grader Celsius. I stedet dannes noen sekret-organeller fra det samme gensettet. men dette sekretet, liksom pestbakterien (type III av TTSS), er en degenerasjon av bakterieflagellen. Minnich sier at selv om bakterieflagellen er mer kompleks, så kom den først, og kunne ikke ha utviklet seg fra TTSS. Dette virker fornuftig: Flagellens mekanisme er dannet for å trekke ut proteinene som flagellen krever på en systematisk måte. Om den blir satt delvis ut spill, så kan den slå ut proteiner (inkl. toksiner) på en tilfeldig måte, slik som TTSS gjør.
Her fokuserer vi mest på roterende motorer, fordi de spesifikt oppfyller Haldanes falsifikasjons-kriterier av evolusjon. Men det finnes også andre typer motorer:
Andre motorer- Kinesin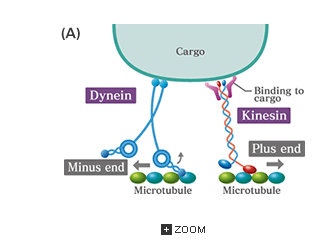
Dette er en miniatyrmotor, som transporterer store molekyler og komponenter gjennom en celle. De 'går' i retning langs mikrotubulens spor, og bruker ett molekyl ATP for hvert trinn de tar. Hvert 'steg' er bare på 8 nm, eller 125 tusen steg pr. mm. Kinesin er et proteinmolekyl, som består av to 'tunge' og to 'lette' kjeder. (Henviser til Bilde 5). Det er mest sannsynlig at de benytter 'overleveringsmekanismer', der kinesinet overtar for hverandre i å knytte seg til tubulen, i det de alternerer i førerposisjon. En ekspert skrev: "Kinesin, et essensielt motorprotein, som flytter intracellulær last, langs mikrotubuler, og går som en person. Nylig arbeid viser at kinesin deler alle kjennetegn på å gå med to føtter. "Utfordringen nå er å bestemme hvordan nytten til denne lilleputt-tofotingen blir koordinert". (29) Kinesin er også kjent for å være vital for celledeling, som livet ikke kan klare seg foruten.
Bilde 5. Kinesin og dynein
Dynein
Kinesin går mot 'pluss-enden' av mikrotubulen, som vanligvis er utover fra senteret. Til å frakte noe den andre veien, benyttes lineære motorer som kalles dynein, som beveger seg mot minus-enden, vanligvis mot senteret i cellen.
Cilia
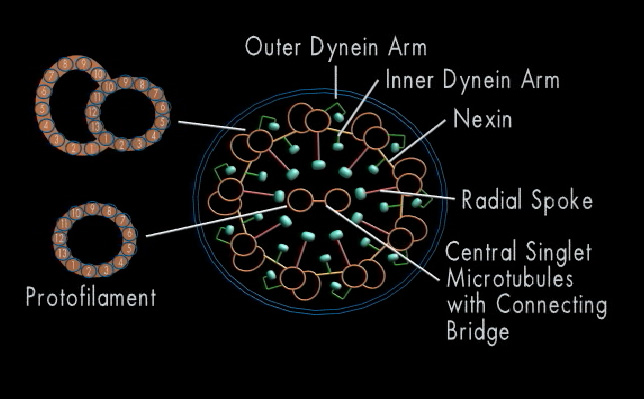
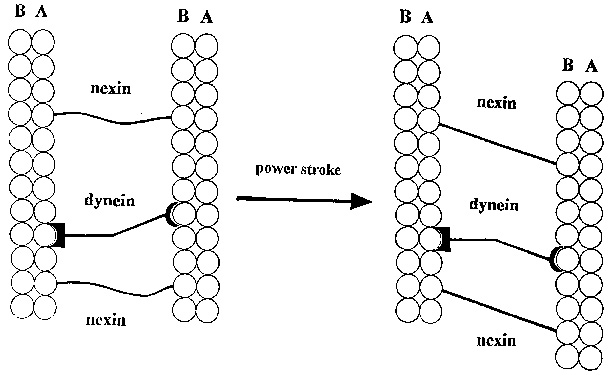 Dynein, nevnt ovenfor, kalles cytoplasma dynein. En annen type motor kalles axoneme: den sentrale element til ett cilium, eller bakterieflagellen. Det er sammensatt som ett lag av mikrotubuler: en røraktig struktur som er tilstede typisk i ni par rundt to enkeltstående, sentrale, i cellens cytoplasma (Se Bilde 7-under). Axoneme utgjør på en måte skjelettet til 'pisklignende' vedheng, som omgir f.eks. bronkiene og eggstokkene. Når dynein spaserer, knytter den seg til to nærliggende mikrotubuler. Disse ville skli bort fra hverandre, om de ikke fantes et fleksibelt 'lenke-protein', nexin (Bilde 6 -til venstre). Det fører til at mikrotubulene bøyer seg, i forhold til hverandre. Resultatet er de regelmessige 'slagene' til cilia, som observeres i mikroskop (30). Cilia er vitale for mange livsfunksjoner, deres koordinerte 'slag' hjelper å flytte 'guffe' fra lungene og i kvinnelige pattedyrs/menneskers eggledere. De leder det befruktede egget til livmoren, hvilket forhindrer det fra å implanteres i egglederne, -som er dødelig.
Dynein, nevnt ovenfor, kalles cytoplasma dynein. En annen type motor kalles axoneme: den sentrale element til ett cilium, eller bakterieflagellen. Det er sammensatt som ett lag av mikrotubuler: en røraktig struktur som er tilstede typisk i ni par rundt to enkeltstående, sentrale, i cellens cytoplasma (Se Bilde 7-under). Axoneme utgjør på en måte skjelettet til 'pisklignende' vedheng, som omgir f.eks. bronkiene og eggstokkene. Når dynein spaserer, knytter den seg til to nærliggende mikrotubuler. Disse ville skli bort fra hverandre, om de ikke fantes et fleksibelt 'lenke-protein', nexin (Bilde 6 -til venstre). Det fører til at mikrotubulene bøyer seg, i forhold til hverandre. Resultatet er de regelmessige 'slagene' til cilia, som observeres i mikroskop (30). Cilia er vitale for mange livsfunksjoner, deres koordinerte 'slag' hjelper å flytte 'guffe' fra lungene og i kvinnelige pattedyrs/menneskers eggledere. De leder det befruktede egget til livmoren, hvilket forhindrer det fra å implanteres i egglederne, -som er dødelig.
Bilde 6. Virkning til nexin
 Cilienes kompleksitet har i det senere vist seg å være enda større. Innen ciliet, så finnes det et presist koordinert system, med IntraFlagellar Transport (IFT). Det involverer kinesin som vandrer opp og ned en intern gangvei. Dette er essensielt både for å bygge og vedlikeholde cilia. Disse frakter en IFT-partikkel, som er en container laget av en 16 proteins-sammensetning. Dette tar tak i nødvendige proteiner, og frigjør det på rett sted og tid {Fascinerende å tenke over hvordan det kan vite om det -oversetters kommentar.}
Cilienes kompleksitet har i det senere vist seg å være enda større. Innen ciliet, så finnes det et presist koordinert system, med IntraFlagellar Transport (IFT). Det involverer kinesin som vandrer opp og ned en intern gangvei. Dette er essensielt både for å bygge og vedlikeholde cilia. Disse frakter en IFT-partikkel, som er en container laget av en 16 proteins-sammensetning. Dette tar tak i nødvendige proteiner, og frigjør det på rett sted og tid {Fascinerende å tenke over hvordan det kan vite om det -oversetters kommentar.}
Bilde 7. Tverrsnitt av cilie
Myocin og actin
Dette motorsystemet er ansvarlig for muskel-sammentrekning. Myocin er en annen motor som inneholder to 'hoder'. Den går, og har en spesiell haleregion. Haleregionen tillater myosiner å samvirke i en tykk tråd, der hodene stikker ut. Når myocin-molekyler 'går' nedover actin-tråder, så er de tilknyttet to Z-linjer i basis-enheten til muskel-fibertråden (se Bilde 8). Myocinets vandring resulterer i at tråder, trekker de to Z-linjene nærmere hverandre, som resulterer i en muskelkontraksjon -se Bilde 8 (til høyre).
Bilde 8. Filament som trekker seg sammen
Virus-motorer for kveiling av DNA
Virus er partikler som er for små til å se under ordinære lysmikroskop, og en trenger elektronmikroskop. Virus kommer i mange ulike størrelser, form og design, og de opererer på ulike måter. De er sammensatt av DNA -eller RNA, i tilfelle RNA-virus, samt protein. De er ikke i stand til å utføre ordinært stoffskifte, heller ikke å reprodusere seg. De er biologisk inaktive, inntil de havner inni vertsceller. Da starter de å reprodusere seg selv, i det de benytter vertscellens ressurser. Den infiserte cellen produserer mange kopier av viruset, og deler seg ofte slik at virusets syklus kan gjentas. En av de vanligste måtene skjer ved å infisere bakterier. Viruset består av et infisert 'halestykke' av protein, og ett proteinskall som inneholder sammenpresset DNA, ved så høyt trykk at når det løsner så presses DNA inn i vertscellen og infiserer den.
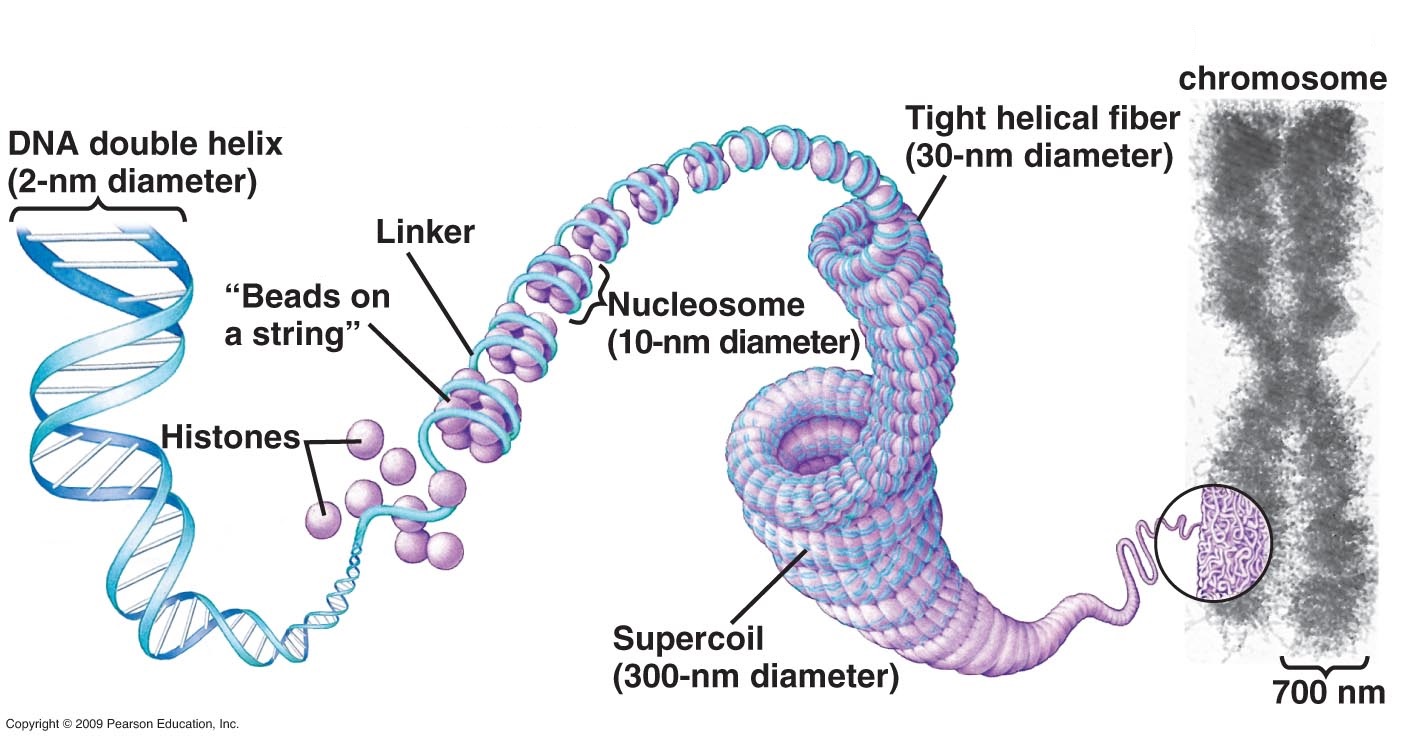 For å klare dette, har viruset en spesiell 'pakkingsmotor, mer kraftig enn noen molekylær motor som er oppdaget, inkludert i muskler. Douglas Smith, ass. professor i fysikk ved UCSD, forklarer utfordringen: "Genomet er ca. 1000 ganger lengre enn virusets diameter. Det tilsvarer å spole og pakke inn over 90 m. fiskesnøre i en kaffekopp, og viruset er i stand til å pakke sitt DNA på under 5 minutter" (33). Smith og kolleger ved UCSD hjalp å løse problemet med hvordan dette gikk til. De analyserte T4, et virus som infiserer E-coli bakterien. De låste laser på ett DNA-molekyl, og målte kraften som ble utøvd på det ut fra virusets 'kveilings-motor'. De viste at motoren utøver en kraft på over 60 pico-newton. Dette høres ikke mye ut (6*10opphøyd i -11 N), men i forhold til størrelsen er det dobbelt så kraftig som en bilmotor. Så motoren, ett enzym-kompleks, kan fange opp og starte å pakke ett DNA-molekyl innen få sekunder.' (30). En slik kraftig motor må bruke mye energi, og i løpet av ett sekund benytter den over 300 enheter av livets energi måleenhet (ATP-syntase). Viruset hadde ett komplementært motorenzym, bygd inn i sin 'pakke-motor' for å frigjøre ATP-energien (35). Og pakkemotoren kan også skifte gir'. Forskerne sier at dette er viktig fordi DNA som den mottar fra cellen, sannsynligvis ikke er en rett, utstrakt snor. Dr. Smith sier: "Akkurat som det er bra for en bil å ha bremser og gir, heller enn bare å fortsette i konstant fart 60 km/t, så kan DNA-pakkemotoren trenge å saktne farten og stoppe, samt vente om den møter en hindring. (33) En rapport sa: "Det kan tillate DNA reparasjon, transkripsjon eller rekombinasjon .. før det genetiske materialet pakkes inn i proteinfrakken (33).
For å klare dette, har viruset en spesiell 'pakkingsmotor, mer kraftig enn noen molekylær motor som er oppdaget, inkludert i muskler. Douglas Smith, ass. professor i fysikk ved UCSD, forklarer utfordringen: "Genomet er ca. 1000 ganger lengre enn virusets diameter. Det tilsvarer å spole og pakke inn over 90 m. fiskesnøre i en kaffekopp, og viruset er i stand til å pakke sitt DNA på under 5 minutter" (33). Smith og kolleger ved UCSD hjalp å løse problemet med hvordan dette gikk til. De analyserte T4, et virus som infiserer E-coli bakterien. De låste laser på ett DNA-molekyl, og målte kraften som ble utøvd på det ut fra virusets 'kveilings-motor'. De viste at motoren utøver en kraft på over 60 pico-newton. Dette høres ikke mye ut (6*10opphøyd i -11 N), men i forhold til størrelsen er det dobbelt så kraftig som en bilmotor. Så motoren, ett enzym-kompleks, kan fange opp og starte å pakke ett DNA-molekyl innen få sekunder.' (30). En slik kraftig motor må bruke mye energi, og i løpet av ett sekund benytter den over 300 enheter av livets energi måleenhet (ATP-syntase). Viruset hadde ett komplementært motorenzym, bygd inn i sin 'pakke-motor' for å frigjøre ATP-energien (35). Og pakkemotoren kan også skifte gir'. Forskerne sier at dette er viktig fordi DNA som den mottar fra cellen, sannsynligvis ikke er en rett, utstrakt snor. Dr. Smith sier: "Akkurat som det er bra for en bil å ha bremser og gir, heller enn bare å fortsette i konstant fart 60 km/t, så kan DNA-pakkemotoren trenge å saktne farten og stoppe, samt vente om den møter en hindring. (33) En rapport sa: "Det kan tillate DNA reparasjon, transkripsjon eller rekombinasjon .. før det genetiske materialet pakkes inn i proteinfrakken (33).
Å benytte cellens maskiner i menneske-tilvirket nano-teknologi
En interessant artikkel erklærte nylig i abstraktet (36): "Den biologiske cellen er utstyrt med en variasjon av molekylære maskiner, som utøver komplekse mekaniske oppgaver, slik som celledeling og intracellulær transport. En kan se for seg å benytte slike biologiske motorer i kunstige omgivelser. Vi går gjennom fremgangen som er oppnådd i å benytte motorproteiner, for å gi energi eller manipulere nano-komponenter. Spesielt kinesin og myosin-motorer som beveger seg langs to lineære tråder er utforsket som aktive komponenter. Mange nåværende applikasjon er kun ment som eks. på nyttig-gjøring, men tilgjengelighet til en hel 'ferdig-til-bruk' verktøyboks med biologiske motorer av nano-format, er en stor anledning som kaller på utforsking." I.e. teknologien i levende organismer er en stor inspirasjon for menneskelige designere, men praktiske applikasjoner er ennå ikke tilgjengelige {da boka ble skrevet, år 2008 -oversetters merknad}.
Siden slike biologiske maskiner på fundamentalt vis ligner våre maskiner, er det ikke ufornuftig å behandle slike motorer også som designet. I virkeligheten er design-teori mer av ett insentiv til å finne ut hvordan delene fungerer, mens forsikringer om evolusjon, ikke bidrar med noe til å benytte dem som maskiner. Artikkelen gir en rekke lovende eks. på bruk, og konkluderer så: "Den vesle størrelsen og kraft-utøvende evner ved slike motorer og raden av muligheter for spesifikk ingeniørkunst, gir disse unike fordeler over nåværende menneskelig-tilvirkede motorer. Ved å studere og benytte biomotorer, vil vi samle mye kunnskap som er av interesse for biologi, materialkunnskap og kjemi. Det er også naturlig å forvente 'spin-off' effekter i medisin, sensorer, elektronikk og ingeniørkunst. Utforsking av biomoterer i teknologien, vil således forbli en tverr-vitenskapelig lekegrind i mange år framover.
Oppsummering
Menneske-tilvirkede motorer viser åpenbar design som ingen vil betvile. Tidligere biologer trodde at hjulet, og desto mer motorer ikke kunne finnes i levende organismer, fordi evolusjon ikke kunne bygge {og bevare dem -oversetters tilføyelse}. Likevel har nåværende forskning oppdaget mange eks. på fantastiske miniatyr-motorer. Spesielt produserer ATP-motoren den vitale livsenergien, som livet ikke kunne eksistert for uten.
Referanser:
1.Dewar, D, Davies, L.M og Haldane J.B.S, Is Evolution a Myth? A debatt mellom D.Dewar og L.M.Davies vs. J.B.S. Haldane, s.90; Watts & Co. Ltd, Paternoster Press, London, 1949
2. Hogan, H. Invasion of the micromachines. Se også: http://creation.com/design-in-living-organisms-motors-atp-synthase
4. Hiroyuki Noyi et al, Direct obervation of the F1-ATPase, Nature 386(6622): 299-302, 1997
5. Block, S. Real engines of creation commentary on Noji, Ref. 4, Nature, 386 86622): 217-219; 1997
6. Wu, C, Molecular engines spins out energy for cells, Science News 151(12: 173, 1997
7. Det skal være fotskrift 0, ikke liten o.
8. Boyer, P., Biophys Acta 1140: 215-250; 1993
9. Abrahams, J.P. et al, Structure at 2.8 A resolution of FA-ATPase from bovine heart niochondria. Nature 370 86491): 621-628; kommentar av Cross, R.L. Our primary source of ATP, same issue ss.594-595
10. Service R.F., Awards for High-Energi Molecules and Cool Atoms, Science 278 (5338): 578-570, 1997
11.Mitome N. et al, Thermophilic ATP synthase har en c-ring: Indication of noninteger 10:3 H+/ATP-ratio and permissive elastic coupling, Proc. Noat. Acad Sci. USA 101(33): 12159-12164
13. ATP-syntase an interpretation. SE ANIMASJON på siden: http://www.iubmb-nicholson.org/atpase.html
14. Bianchet, M.A. et al., The 2.8-Å structure of rat liver F1-ATPase
15. Bergman, J. ATP: The perfect energy currency for the cell, Dreation Res. Soc. Q 36(1)2-10, 1999; http://creation.com/design-in-living-organisms-motors-atp-synthase
16. Researchers solve mystery of how DNA-strands separate, physorg.com/news102663442.html
17. Etter R. Dawkins bok: 'Climbing Mount Improbable (1996): gjennomgang av Sarfati på : http://creation.com/book-review-of-dawkins-climbing-mount-improbable
18. En god oppsummering av Howard Berg, professor i molecular and cellular biology, and of physics, ved Harvard University: Motile Behaviour of Bacteria, Physics Today, 1999.
19. http://creation.com/15-ways-to-refute-materialistic-bigotry
20. En nyere versjon av Millers argument er: Miller, K.R., The Flagellum Unspun: The Collapse of 'Irreducible Complexity'; in Dembski, W.A. og Ruse M., red, Debating Design: From Darwin to DNA, Cambridge University Press, 2004.
21. http://creation.com/misotheists-misology-richard-dawkins-attacks-michael-behe
22.Unlocking the Mystery of Life, DVD, Illustra Media, 2002
29. Ashbury, C.L., Kinesin: worlds tiniest biped, Curr. Opinion Cell Biol 17:89-97, 2006
30. http://arn.org/docs/behe/mb_mm92496.htm
33. Powerful Molecular Motors Permits Speedy Assembly of Viruses, Physorg.com, 2007
35. SunS. et al., The Structure of the ATPase that Powers DNA Packaging into Bacteriohage T4 Procapsids, Molecular Cell 25:943-949, 2007
36. van den Heuvel, M.G.L.og Dekker, C. Motor Proteins at Work for Nanotechnology, Science 317 (5836): 333-336; 2007
Stoffutvalg og bilder ved Asbjørn E. Lund
 Den levende verden inneholder overraskende nok skikkelige elektriske, rotasjonsmotorer. For evolusjonister som forutsa at hjul ikke kunne eksistere, fordi de ikke kunne ha utviklet seg gradvis, må de være et tankekors. Motorene i den levende verden, er perfekte eks. på den ultimate nano-teknologi. Biosfæren har også en variasjon av lineære motorer, som er like problematiske for evolusjonsteorien. I noe banebrytende forskning benyttes biologiske motorer for å assistere menneske-tilvirket nanoteknologi, som for tiden er primitiv sammenlignet med maskiner i biosfæren.
Den levende verden inneholder overraskende nok skikkelige elektriske, rotasjonsmotorer. For evolusjonister som forutsa at hjul ikke kunne eksistere, fordi de ikke kunne ha utviklet seg gradvis, må de være et tankekors. Motorene i den levende verden, er perfekte eks. på den ultimate nano-teknologi. Biosfæren har også en variasjon av lineære motorer, som er like problematiske for evolusjonsteorien. I noe banebrytende forskning benyttes biologiske motorer for å assistere menneske-tilvirket nanoteknologi, som for tiden er primitiv sammenlignet med maskiner i biosfæren. lokkerte arterier og blod-rensing, så gjør antall deler det vanskelig å lage dem, under en viss størrelse. Men oppfinnsomme ingeniører gjør dem mindre hele tiden (2).
lokkerte arterier og blod-rensing, så gjør antall deler det vanskelig å lage dem, under en viss størrelse. Men oppfinnsomme ingeniører gjør dem mindre hele tiden (2).
 Bakterien drives ved hjelp av reelle elektriske, utenbords-motorer, som bare er 45 nanometer i diameter (14). Disse motorene er forbundet med lange, tynne, pisk-lignende skrueformede tråder, som er flere ganger lengre enn mikroben, via ett universal-ledd. Dette omgjør den roterende bevegelsen til en bølgeliknende bevegelse i tråden. Motoren innbefatter en stator, rotor, drivaksel og en hylse som leder drivakselen ut av celleveggen. Samlingen av motor og tråd kalles en bakterie-flagell (14). Cellen har flere flageller og deres samvirkende fremdrift tillater cellen å svømme 35 cellers lengde pr. sekund (14). I likhet med ATP-syntase motoren blir den drevet av en proton-flyt, denne gang fra utsiden til innsiden av delen (unntatt marine-bakterier og bakterier i meget alkaliske betingelser, der sodium-ioner benyttes i stedet.) Protonene drivers enten av en elektrisk eller en pH-gradient, og energien til å drive den er fra oksidasjon av næringen dens. Proton-flyten endrer formen til én av deres stator-proteiner, som utvirker en kraft på en av rotor-proteinene, og derved driver rotoren rundt (14).
Bakterien drives ved hjelp av reelle elektriske, utenbords-motorer, som bare er 45 nanometer i diameter (14). Disse motorene er forbundet med lange, tynne, pisk-lignende skrueformede tråder, som er flere ganger lengre enn mikroben, via ett universal-ledd. Dette omgjør den roterende bevegelsen til en bølgeliknende bevegelse i tråden. Motoren innbefatter en stator, rotor, drivaksel og en hylse som leder drivakselen ut av celleveggen. Samlingen av motor og tråd kalles en bakterie-flagell (14). Cellen har flere flageller og deres samvirkende fremdrift tillater cellen å svømme 35 cellers lengde pr. sekund (14). I likhet med ATP-syntase motoren blir den drevet av en proton-flyt, denne gang fra utsiden til innsiden av delen (unntatt marine-bakterier og bakterier i meget alkaliske betingelser, der sodium-ioner benyttes i stedet.) Protonene drivers enten av en elektrisk eller en pH-gradient, og energien til å drive den er fra oksidasjon av næringen dens. Proton-flyten endrer formen til én av deres stator-proteiner, som utvirker en kraft på en av rotor-proteinene, og derved driver rotoren rundt (14). 
 Dynein, nevnt ovenfor, kalles cytoplasma dynein. En annen type motor kalles axoneme: den sentrale element til ett cilium, eller bakterieflagellen. Det er sammensatt som ett lag av mikrotubuler: en røraktig struktur som er tilstede typisk i ni par rundt to enkeltstående, sentrale, i cellens cytoplasma (Se Bilde 7-under). Axoneme utgjør på en måte skjelettet til 'pisklignende' vedheng, som omgir f.eks. bronkiene og eggstokkene. Når dynein spaserer, knytter den seg til to nærliggende mikrotubuler. Disse ville skli bort fra hverandre, om de ikke fantes et fleksibelt 'lenke-protein', nexin (Bilde 6 -til venstre). Det fører til at mikrotubulene bøyer seg, i forhold til hverandre. Resultatet er de regelmessige 'slagene' til cilia, som observeres i mikroskop (30). Cilia er vitale for mange livsfunksjoner, deres koordinerte 'slag' hjelper å flytte 'guffe' fra lungene og i kvinnelige pattedyrs/menneskers eggledere. De leder det befruktede egget til livmoren, hvilket forhindrer det fra å implanteres i egglederne, -som er dødelig.
Dynein, nevnt ovenfor, kalles cytoplasma dynein. En annen type motor kalles axoneme: den sentrale element til ett cilium, eller bakterieflagellen. Det er sammensatt som ett lag av mikrotubuler: en røraktig struktur som er tilstede typisk i ni par rundt to enkeltstående, sentrale, i cellens cytoplasma (Se Bilde 7-under). Axoneme utgjør på en måte skjelettet til 'pisklignende' vedheng, som omgir f.eks. bronkiene og eggstokkene. Når dynein spaserer, knytter den seg til to nærliggende mikrotubuler. Disse ville skli bort fra hverandre, om de ikke fantes et fleksibelt 'lenke-protein', nexin (Bilde 6 -til venstre). Det fører til at mikrotubulene bøyer seg, i forhold til hverandre. Resultatet er de regelmessige 'slagene' til cilia, som observeres i mikroskop (30). Cilia er vitale for mange livsfunksjoner, deres koordinerte 'slag' hjelper å flytte 'guffe' fra lungene og i kvinnelige pattedyrs/menneskers eggledere. De leder det befruktede egget til livmoren, hvilket forhindrer det fra å implanteres i egglederne, -som er dødelig.  Cilienes kompleksitet har i det senere vist seg å være enda større. Innen ciliet, så finnes det et presist koordinert system, med IntraFlagellar Transport (IFT). Det involverer kinesin som vandrer opp og ned en intern gangvei. Dette er essensielt både for å bygge og vedlikeholde cilia. Disse frakter en IFT-partikkel, som er en container laget av en 16 proteins-sammensetning. Dette tar tak i nødvendige proteiner, og frigjør det på rett sted og tid {Fascinerende å tenke over hvordan det kan vite om det -oversetters kommentar.}
Cilienes kompleksitet har i det senere vist seg å være enda større. Innen ciliet, så finnes det et presist koordinert system, med IntraFlagellar Transport (IFT). Det involverer kinesin som vandrer opp og ned en intern gangvei. Dette er essensielt både for å bygge og vedlikeholde cilia. Disse frakter en IFT-partikkel, som er en container laget av en 16 proteins-sammensetning. Dette tar tak i nødvendige proteiner, og frigjør det på rett sted og tid {Fascinerende å tenke over hvordan det kan vite om det -oversetters kommentar.}
 For å klare dette, har viruset en spesiell 'pakkingsmotor, mer kraftig enn noen molekylær motor som er oppdaget, inkludert i muskler. Douglas Smith, ass. professor i fysikk ved UCSD, forklarer utfordringen: "Genomet er ca. 1000 ganger lengre enn virusets diameter. Det tilsvarer å spole og pakke inn over 90 m. fiskesnøre i en kaffekopp, og viruset er i stand til å pakke sitt DNA på under 5 minutter" (33). Smith og kolleger ved UCSD hjalp å løse problemet med hvordan dette gikk til. De analyserte T4, et virus som infiserer E-coli bakterien. De låste laser på ett DNA-molekyl, og målte kraften som ble utøvd på det ut fra virusets 'kveilings-motor'. De viste at motoren utøver en kraft på over 60 pico-newton. Dette høres ikke mye ut (6*10opphøyd i -11 N), men i forhold til størrelsen er det dobbelt så kraftig som en bilmotor. Så motoren, ett enzym-kompleks, kan fange opp og starte å pakke ett DNA-molekyl innen få sekunder.' (30). En slik kraftig motor må bruke mye energi, og i løpet av ett sekund benytter den over 300 enheter av livets energi måleenhet (ATP-syntase). Viruset hadde ett komplementært motorenzym, bygd inn i sin 'pakke-motor' for å frigjøre ATP-energien (35). Og pakkemotoren kan også skifte gir'. Forskerne sier at dette er viktig fordi DNA som den mottar fra cellen, sannsynligvis ikke er en rett, utstrakt snor. Dr. Smith sier: "Akkurat som det er bra for en bil å ha bremser og gir, heller enn bare å fortsette i konstant fart 60 km/t, så kan DNA-pakkemotoren trenge å saktne farten og stoppe, samt vente om den møter en hindring. (33) En rapport sa: "Det kan tillate DNA reparasjon, transkripsjon eller rekombinasjon .. før det genetiske materialet pakkes inn i proteinfrakken (33).
For å klare dette, har viruset en spesiell 'pakkingsmotor, mer kraftig enn noen molekylær motor som er oppdaget, inkludert i muskler. Douglas Smith, ass. professor i fysikk ved UCSD, forklarer utfordringen: "Genomet er ca. 1000 ganger lengre enn virusets diameter. Det tilsvarer å spole og pakke inn over 90 m. fiskesnøre i en kaffekopp, og viruset er i stand til å pakke sitt DNA på under 5 minutter" (33). Smith og kolleger ved UCSD hjalp å løse problemet med hvordan dette gikk til. De analyserte T4, et virus som infiserer E-coli bakterien. De låste laser på ett DNA-molekyl, og målte kraften som ble utøvd på det ut fra virusets 'kveilings-motor'. De viste at motoren utøver en kraft på over 60 pico-newton. Dette høres ikke mye ut (6*10opphøyd i -11 N), men i forhold til størrelsen er det dobbelt så kraftig som en bilmotor. Så motoren, ett enzym-kompleks, kan fange opp og starte å pakke ett DNA-molekyl innen få sekunder.' (30). En slik kraftig motor må bruke mye energi, og i løpet av ett sekund benytter den over 300 enheter av livets energi måleenhet (ATP-syntase). Viruset hadde ett komplementært motorenzym, bygd inn i sin 'pakke-motor' for å frigjøre ATP-energien (35). Og pakkemotoren kan også skifte gir'. Forskerne sier at dette er viktig fordi DNA som den mottar fra cellen, sannsynligvis ikke er en rett, utstrakt snor. Dr. Smith sier: "Akkurat som det er bra for en bil å ha bremser og gir, heller enn bare å fortsette i konstant fart 60 km/t, så kan DNA-pakkemotoren trenge å saktne farten og stoppe, samt vente om den møter en hindring. (33) En rapport sa: "Det kan tillate DNA reparasjon, transkripsjon eller rekombinasjon .. før det genetiske materialet pakkes inn i proteinfrakken (33).